Foto: ChatGPT
Introducción
Los arrecifes de coral, que son cruciales para la salud y la diversidad del ecosistema marino mundial, han experimentado una disminución considerable en las últimas 2 décadas debido a las actividades humanas y el cambio climático. Según el informe Status of Coral Reefs of the World: 2020, aproximadamente el 14% de los arrecifes de coral globales se perdieron entre 2009 y 2018 debido al aumento de las temperaturas oceánicas, la acidificación y la contaminación. 1[1]. Los frecuentes eventos de blanqueamiento de coral, impulsados por el aumento prolongado de la temperatura del mar, han tenido efectos devastadores en los ecosistemas de arrecifes 2[2]. Los episodios de blanqueamiento masivo de corales en 1998, 2010 y 2015 impactaron colectivamente más del 70% de los arrecifes de coral en todo el mundo, subrayando la urgencia de las estrategias de conservación 3[3,4]. Se 56ha empleado la crioconservación, un método para preservar materiales biológicos a bajas temperaturas para garantizar que sus funciones vitales y su viabilidad permanezcan intactas tras la descongelación [5,6,7], en una variedad de sustancias, tales como gametos de coral y material genético de peces 8[8,9]. Esta técnica es prometedora para la conservación de especies en peligro de extinción y para facilitar los avances en biología del desarrollo y la biotecnología marina [10,11]. A pesar de su potencial, la criopreservación plantea desafíos formidables. Por ejemplo, los cristales 13de hielo pueden formar [12,13], lo que puede resultar en daños a las células y tejidos y aumentar el riesgo de contaminación por agentes patógenos [14]. La vitrificación, un método avanzado de crioconservación, enfría rápidamente las muestras biológicas a temperaturas de congelación en un medio similar al vidrio, evitando la formación de cristales de hielo. Aunque la vitrificación aún no está ampliamente establecida en la crioconservación acuática, se ha aplicado experimentalmente a un número limitado de especies de invertebrados y ofrece ventajas potenciales sobre los métodos de enfriamiento lento, incluidos los requisitos simplificados del equipo y los tiempos de procesamiento más cortos 8[8].
Materiales y métodos
Recogida de coral y aislamiento de ovocitos
Los especímenes de J. fragilis y J. juncea se recogieron durante su temporada reproductiva (junio-septiembre) del Parque Nacional de Kenting, Nanwan, Taiwán (21°56’N, 120°44’E) a profundidades de 3–10 m. La Oficina Nacional de Administración de Parques de Kenting de Taiwán emitió un permiso de recolección de coral a los autores del estudio. Posteriormente, los buceadores profesionales recolectaron las cantidades permitidas de las sucursales de J. fragilis y J. juncea, que luego fueron transportadas al centro de cría de coral del Museo Nacional de Biología Marina y Acuario en Checheng, Taiwán. A su llegada, las ramas se fijaron a sustratos con fijaciones y se colocaron en tanques de media tonelada con bases de grava. Se hizo circular agua de mar nativa con una salinidad de 35 ppt a través de los tanques, que se mantuvieron a una temperatura constante de 25°C. Cada rama midió aproximadamente 60 cm y se analizó y categorizó por tipo y cantidad de ovocitos antes de ser transferida a la instalación de cría.
Efectos de la solución de vitrificación sobre los ovocitos
Las concentraciones de CPAs usados en la producción de la Solución de Equilibración 1 (ES1), ES2 y VS se presentan en la Tabla 1. Estas soluciones prepararon secuencialmente los oocitos para la exposición al VS. Esta fase experimental se usó para evaluar la toxicidad de ES1 (propilenglicol (1 M (PG) + etilenglicol (EG) 0,25 M + metanol 0,5 M), ES2 (2 M PG + 0,5 M EG + 1 M metanol) y VS (4 M PG + 1 M EG + 2 M metanol) a los ovocitos. En cada experimento, se sumergieron 30-50 ovocitos recién cosechados en una de las tres soluciones en un plato de cultivo de seis pocillos. Para ES1 y ES2, se retiraron cinco ovocitos a tres intervalos: 5, 10 y 15 minutos. Se utilizaron recuentos de ATP para determinar la viabilidad de los ovocitos. Se sometieron cinco oocitos a pruebas de viabilidad en VS a intervalos de 2, 4 y 8 minutos. Estos experimentos se llevaron a cabo en dos condiciones de temperatura: temperatura ambiente (26°C) y un baño de hielo (5°C).
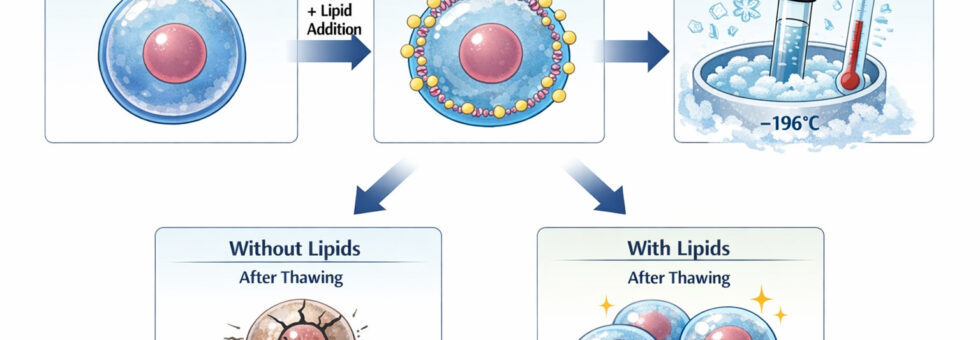
Incorporación de liposomas en VS para la vitrificación
Para investigar el efecto de la composición lipídica sobre la criotolerancia a los ovocitos, se seleccionaron nueve tipos de lípidos basándose en sus funciones estructurales en las membranas celulares y las propiedades crioprotectoras previamente reportadas en gametos y embriones. Los lípidos incluían fosfolípidos (PLs: fosfatidilcolina (PC) y fosfatidiletanolamina (PE), ácidos grasos monoinsaturados (MUFA: ácido erúcico, ácido oleico, ácido palmitoleico) y ácidos grasos poliinsaturados (PUFA: ácido docosahexaenoico, ácido linoleico y ácido eicosatrienoico). Los PL como PC y PE son parte integral de las membranas de ovocitos de coral e influyen en la integridad de la membrana en condiciones de baja temperatura. Los MUFA se eligieron por su capacidad para mantener la fluidez de la membrana y reducir la lesión por enfriamiento, mientras que los PUFA se incluyeron debido a sus beneficios reportados en los modelos de crioconservación de vertebrados, aunque sus efectos en los invertebrados marinos siguen siendo inciertos.
Fuente de información:
Link de la nota: La incorporación de lípidos mejora la criotolerancia de los ovocitos de coral de gorgonia vitrificada
Autores: Yen-Po Chen, Tzu-Fei Huang, Ester Lo, Sujune Tsai, Zhi-Hong Wen, Hung-Kai Chen, Chiahsin Lin
Foto ©: ChatGPT
Copyright © 2026 Smithsonian. Todos los derechos reservados.